胰腺癌,也許是免疫治療最難啃的一塊硬骨頭。
厚重的細胞外基質作為防護殼,抑制性極強的免疫微環境,加上狡詐多端的癌細胞,此前所向披靡的PD-1抑製劑,也沒法上演單騎救主的好戲。
但是我們還有“協同作戰”這一招。近期公佈的臨床試驗 COMBAT(KEYNOTE-202)的數據顯示,新型CXCR4抑製劑BL-8040(Motixafortide),配合PD-1抑製劑和化療聯合使用,在胰腺癌的二線/三線治療中初步效果良好。
這種三聯療法,在試驗中作為二線治療使用,疾病控制率達到77%,其中35%的患者實現了客觀緩解,緩解持續時間達到7.8個月,這些數據都是胰腺癌治療多年來難得的進步 [1]。相關數據發表在《自然·醫學》上。
看到Review上的新藥出成績,不錯不錯
(圖片來源:Nature Reviews Clinical Oncology)
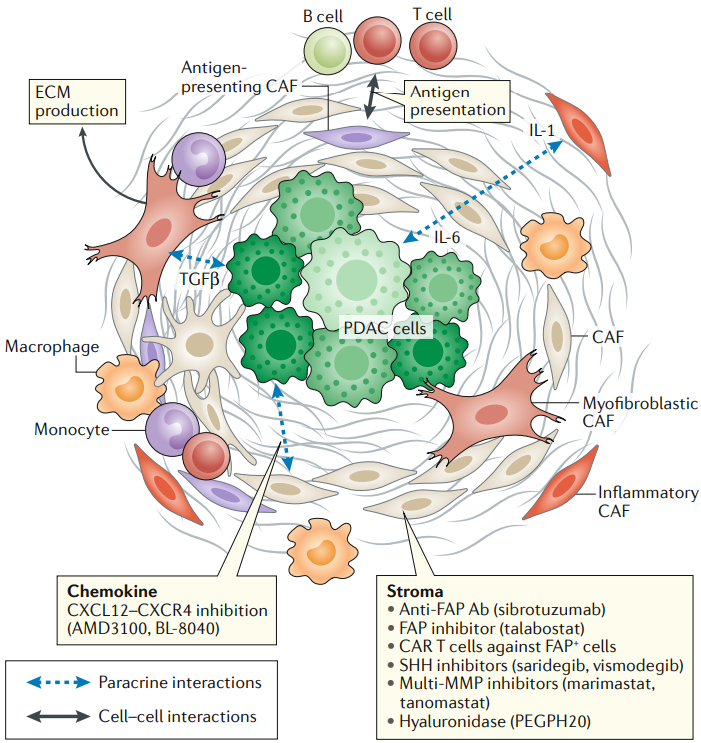
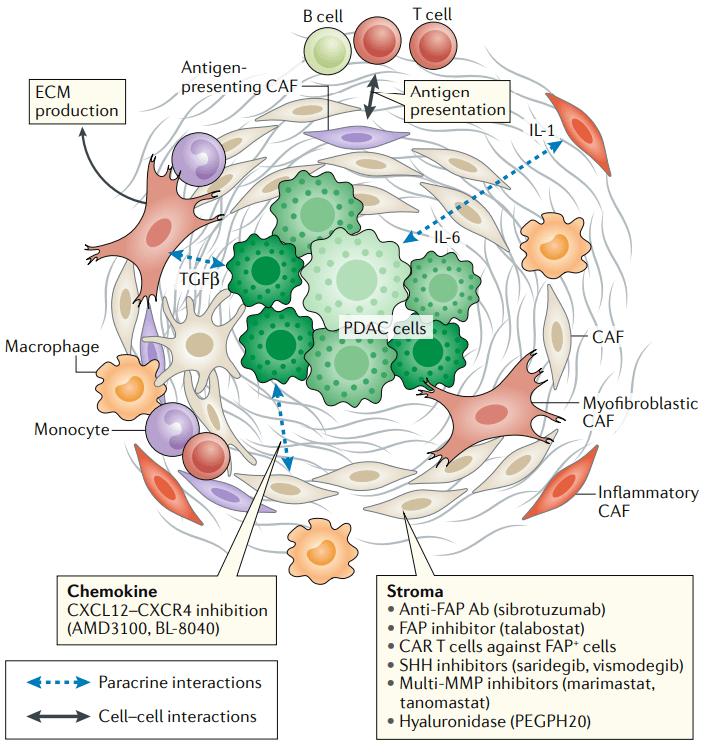
對於胰腺癌為什麼難治,科學家們已經總結出了不少原因,其中很重要的一條就是腫瘤微環境當中,CD8+T細胞的數量實在是太少。即使免疫檢查點抑製劑能穿越重重屏障抵達腫瘤部位,也很難調動起足夠強大的抗腫瘤免疫應答[2]。
所以要想讓PD-1抑製劑們具備挑戰胰腺癌的能力,就得給它配上可靠的隊友。本次試驗中使用的CXCR4抑製劑,就是近年來頗受關注的新星,因為很多癌細胞都存在CXCR4的高表達。
具體到胰腺癌的話,抑制CXCR4一方面可以增加腫瘤微環境中T細胞的數量,同時還可以針對一下胰腺癌細胞外基質中,大量存在的腫瘤相關成纖維細胞(CAF)[3-4]。這樣雙管齊下,就能削弱胰腺癌腫瘤微環境對於免疫治療的不利影響。
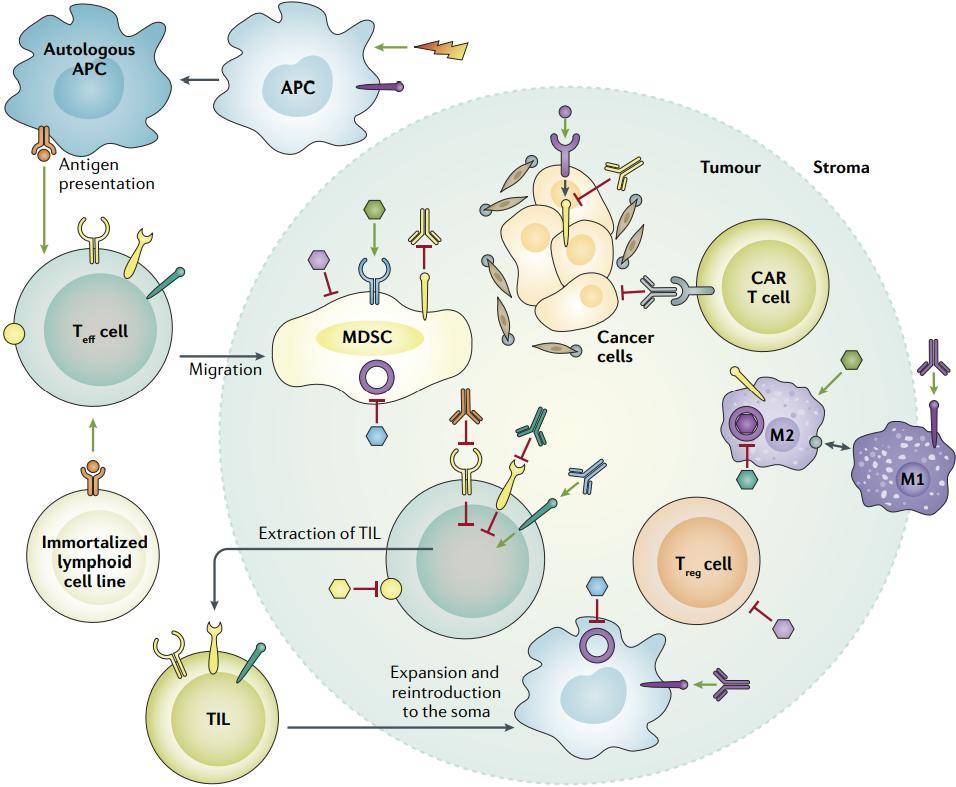
圖上的每一個要素,都可能對免疫治療效果有影響
(圖片來源:Nature Reviews Clinical Oncology)
動物實驗也顯示,PD-1/L1抑製劑與CXCR4抑製劑聯合使用,會存在協作增效性,所以讓這兩種藥物聯手,就是非常自然的選擇了。
接下來就說說COMBAT試驗,這項試驗分為兩部分進行,第一部分先是驗證BL-8040+帕博利珠單抗,作為後線治療的安全性和初步療效。在胰腺癌當中,三線和三線以上的治療難度很大,缺乏成熟的方案。
這部分試驗總共有29名患者參與,BL-8040+帕博利珠單抗的整體疾病控制率為34.5%,只有一名患者達到客觀緩解,這也體現了胰腺癌的“硬骨頭”。
但分析數據顯示,療效主要體現在二線治療的16名患者當中,他們的中位生存期達到7.5個月,明顯優於此前FDA批准的伊立替康脂質體+氟尿嘧啶+亞葉酸鈣方案的生存期(6.1個月)。
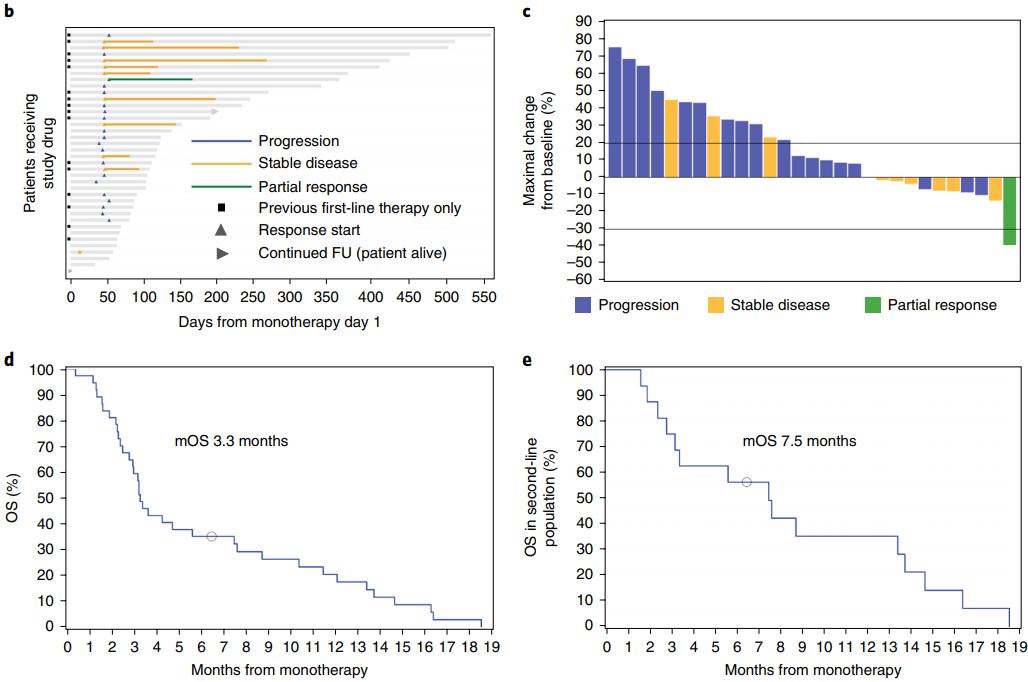
三線及三線以上的患者,把左邊的患者整體生存期拉得好低……
各種檢測結果也提示,BL-8040+帕博利珠單抗的治療,增加了外周血中活化T細胞的水平,減少了調節性T細胞的數量,浸潤到腫瘤內的CD8+T細胞也明顯增多。
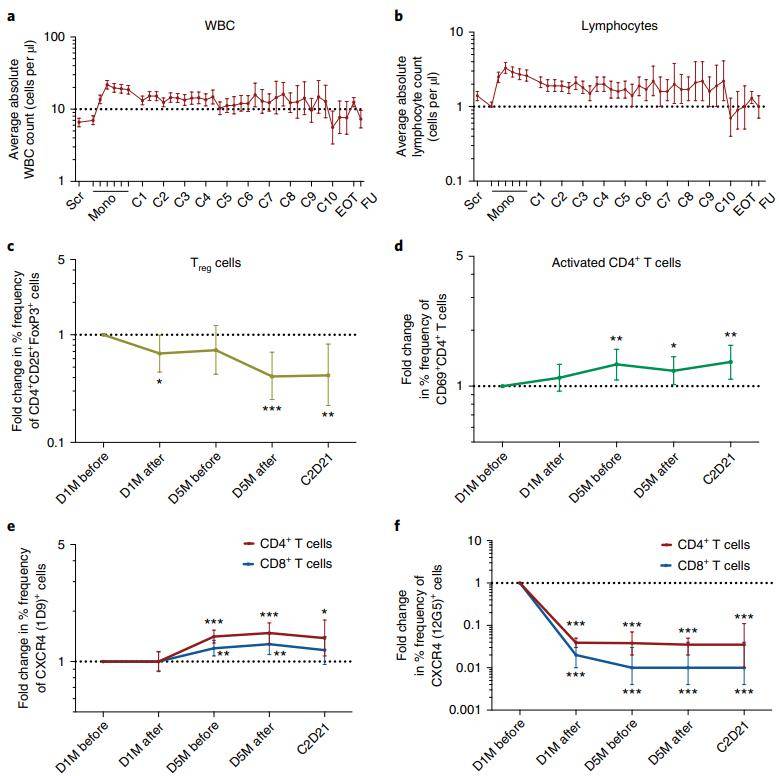
活化T細胞是側面衡量療效的手段
基於這些結果,研究團隊在試驗第2部分專門入組了22名吉西他濱一線治療後,病情出現進展的轉移性胰腺癌患者,在BL-8040+帕博利珠單抗的基礎上,加用伊立替康脂質體+氟尿嘧啶+亞葉酸鈣的三藥化療方案進行治療。
有了化療強力增援,療效立馬就上去了。22名患者中有7名實現部分緩解,客觀緩解率為32%,而中位緩解持續時間達到了7.8個月,明顯優於單純化療。再算上10名治療後病情未進展的患者,整體的疾病控制率(DCR),達到了77%!
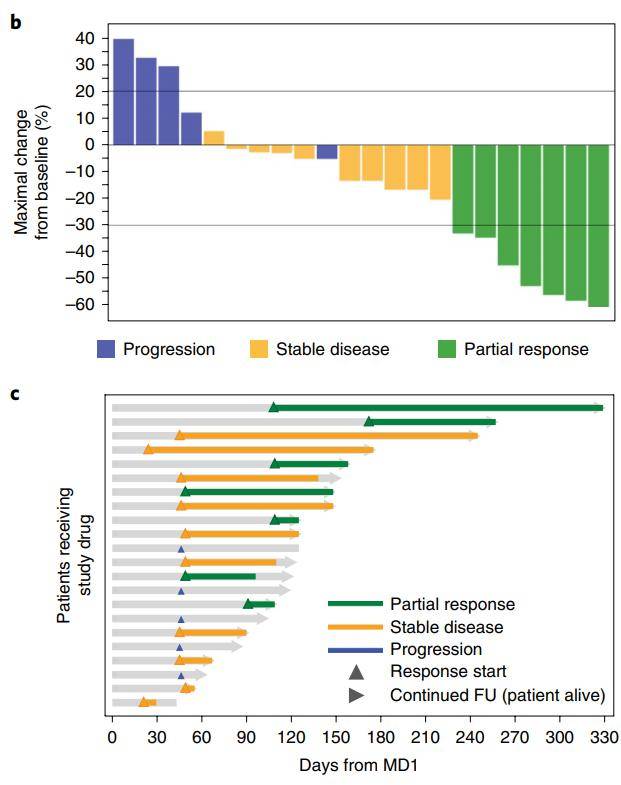
緩解和疾病控制,持續時間都不差嘛
三藥化療方案在此前的臨床III期試驗中,客觀緩解率和疾病控制率分別是17%和52%[5]。而且這22名患者中並不存在微衛星不穩定性高(MSI-H),更適合免疫治療的患者,所以BL-8040+帕博利珠單抗提升的療效就更不易了。
雖然看似用藥很多,但22名患者中只有兩名因為副作用明顯而停藥,3-4級的嚴重不良事件以腹瀉和乏力為主,發生率也比較低。因此研究團隊認為,治療方案也是安全可耐受的。
不過在本次論文中,並沒有公佈試驗第2部分的總生存期(OS)、無進展生存期(PFS)等指標。BL-8040和PD-1抑製劑的搭檔到底能體現多大價值,就有待後續數據和試驗去揭曉啦。
編輯神叨叨
1.Bockorny B, Semenisty V, Macarulla T, et al. BL-8040, a CXCR4 antagonist, in combination with pembrolizumab and chemotherapy for pancreatic cancer: the COMBAT trial [J]. Nature Medicine, 2020.
2.Ho WJ, Jaffee EM, Zheng L. The tumour microenvironment in pancreatic cancer — clinical challenges and opportunities [J]. Nature Reviews Clinical Oncology, 2020.
5.Wang-Gillam A, Li CP, Bodoky G, et al. Nanoliposomal irinotecan with fluorouracil and folinic acid in metastatic pancreatic cancer after previous gemcitabine-based therapy (NAPOLI-1): a global, randomised, open-label, phase 3 trial[J]. The Lancet, 2016, 387(10018): 545-557.