來源:奇點網
「天文學「和「觀星」對大家而言或許是遙遠浪漫的事。
而近日,約翰霍普金斯大學Janis M. Taube領銜的研究團隊在《科學》雜誌的發文[1],則一舉展示了什麼叫做「不懂浪漫的腫瘤成像學不是好研究」~
他們藉助天文成像分析技術開發了一個分析腫瘤切片的平台AstroPath。用AstroPath對接受PD-1抑制劑的98位黑色素瘤病人進行了腫瘤切片分析,發現了兩種與PD-1抑制劑應答顯著相關的腫瘤侵潤免疫細胞:CD163+PD-L1- 髓細胞 (無應答)和 CD8+FoxP3+PD1low/mid T細胞(應答)。
值得一提的是,他們還通過合併AstroPath找到的多種細胞表型,實現了在獨立驗證樣本群中對患者存活率(OS,PFS)的預測。

論文首頁截圖
由於免疫檢查點抑制劑(ICI)在不同腫瘤的臨床應用中只有一小部分患者獲益,因此臨床上急需更好的生物標誌物幫助篩選出受益人群[2]。
單色免疫組織化學(IHC)和免疫熒光染色(IF)使臨床病理檢測在幾十年間取得了巨大的進步,但在預測ICI治療效果方面還存在着許多不足。其中主要原因是,免疫治療應答涉及腫瘤內、微環境內和全身的眾多細胞,以及它們之間的相互作用,單一的標誌物往往不足以概括這其中的複雜關係。比如PD-L1作為獲得FDA批准的ICI生物標誌物,依然無法準確的預測免疫療法應答[3]。
多色免疫組化(mIHC)和免疫熒光染色(mIF)提供了可以呈現和分析多種免疫相關因子的方法(如觀測腫瘤侵潤免疫細胞的表型),是在ICI標誌物研究中一直被看好的技術。
一篇發表於2019年的系統評價和meta分析指出,在近幾年PD-1/PD-L1抑制劑生物標誌物的研究中,相較於IHC和腫瘤突變負荷,mIF/mIHC 測量對免疫應答有更高的預測準確度[4]。
遺憾的是,雖然用mIF研究腫瘤微環境(TME)的研究非常多,但是mIF一直沒能確定一種可標準化的標誌物。這或許是因為mIF在圖像分析和大量數據處理方面面臨着很多挑戰;尤其是在分析面積較大的腫瘤切片時,往往需要研究者進行選區分析,但這會影響對TME細胞組成測量的全面性。
Janis M. Taube團隊意識到,用天文望遠鏡觀測的星系和用顯微鏡觀察的細胞在成像分析上非常相似,於是他們大膽借鑑了用於分析 1022米尺度星系的圖像分割經驗,對在 10-6米尺度上的腫瘤病理圖像分析進行了改革。

天文學的銀河系識別和病理學的腫瘤切片細胞識別有着相通之處
由此建立的AstroPath 平台不僅解決了腫瘤成像分析中許多常見問題,還通過將mIF和其分析流程標準化,推進了這項技術在ICI療法的標誌物發現和臨床篩選中的應用。
Janis M. Taube團隊意識到,如果想通過mIF實現對TME更精準的評估,就不能像以往的腫瘤成像研究那樣將標誌物表達分為陽性或陰性。
於是他們首先對測量參數的可靠性進行了優化,重點解決了熒光信號的強度不穩定,對分子表達於哪種細胞的鑑定不準確(切片有相鄰或重疊細胞,相鄰熒光通道的信號「溢出」造成的信號重疊),以及顯微鏡亮度變化和透鏡畸對原位置信號測量的影響等問題。
研究人員通過反覆試驗,將這些問題一一擊破。例如,對於熒光強度低,無法準確檢測到有PD-L1low表型的細胞,就使用酪酰胺信號放大(TSA-based)技術,並且逐一調整一抗和熒光基團的稀釋度,確保每個標誌物在mIF中的檢測值與IHC顯色檢測(chromogenic IHC)相符。最終設計出了mIF六重標記物檢測組合(PD-1, PD-L1, CD163, FoxP3, CD8, Sox10/S100)。

Astropath在本文中使用的mIF六重檢測組合在信號表達上與IHC顯色檢測相符
在圖像採集上,不完全平場校正(incomplete flat-fielding)會造成熒光強度變化,而拼接錯誤也會造成高倍視野區(HPF)的錯位,這些問題會直接影響4-5% 的細胞分析結果。
作者借鑑了天文觀測中的經驗,在每個HPF之間保留了20%的重疊圖像,並用類似於光學防抖原理的「彈簧模型「把像素偏移最小化。

(B)白色為圖像重疊部分(C)彈簧模型採取了以一個點為基準調整偏移像素
除此以外,作者還對分析細胞表型進行了多次程序優化,解決了mIF成像分析中常見的細胞分割問題。如會把單個較大細胞(例如癌細胞,髓細胞)進行多次分割,從而記錄為多個。
對於優化後的程序,作者也進行了多重把控來保證結果的準確性和可複製性。比如從每個樣本中抽取~25000個細胞進行驗證,以及對照正常組織表達(微陣列)進行校準。這些把控大大減少了mIF研究中常見的批次效應(batch effect),提高了AstroPath的實用性。

AstroPath通過程序優化解決了細胞分割和表型預測上的問題
通過對AstroPath的成功運用,作者在黑色素瘤的腫瘤微環境裏找到了CD8+FoxP3+表型的T細胞(在腫瘤微環境T細胞里僅佔比~3%的稀有亞型),且結合這些T細胞集中於腫瘤邊緣的位置,判斷出它們可能是處於致敏早期的腫瘤反應性T細胞。

腫瘤細胞和不同T細胞亞型在黑色素瘤微環境裏的位置分佈
接下來,作者將AstroPath測量的腫瘤PD-L1表達和傳統病理方法(用IHC進行人工評分)進行了對比。AstroPath mIF測量的PD-L1表達和 PD-L1+腫瘤細胞密度都與ICI應答成正相關,而傳統方法則沒能預測ICI應答。
mIF會產生大量的圖像數據,在一般實驗或臨床應用中很難做到對整個切片進行採集和分析。人工選取HPF則會帶來選擇性偏差,並無法全面分析腫瘤微環境裏的細胞多樣性。於是作者又把目光轉回了在生成大型多光譜數據集方面有着豐富經驗的天文學研究。
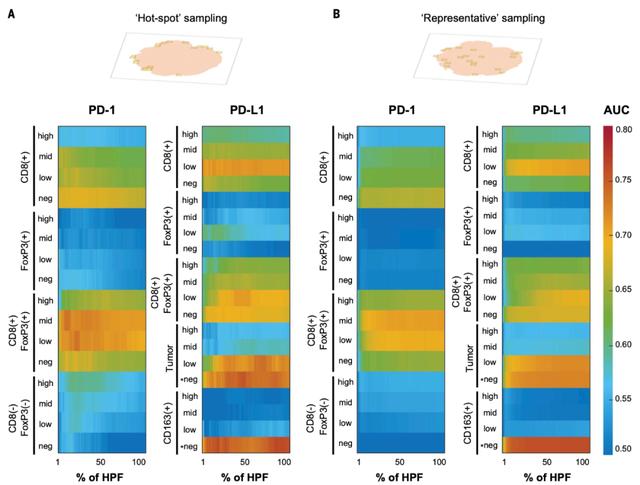
在觀測廣袤的宇宙時,星系可能只是微小的噪點,想確定它們的位置則需要增強信噪比。據此,科研人員們設計出了CD8「熱點」篩選法:根據 CD8+T 細胞的密度對 HPF 進行排名,首先選擇密度最高的,以此找出腫瘤微環境中免疫激活度最高的地方。他們把用熱點發篩選出的HPF,和隨機抽取的HPF進行了標誌物測量的對比。
通過熱點篩選法,作者得出CD8+FoxP3+PD-1low/midT細胞密度和ICI應答成正相關;在僅選取~10-30% 的總切片面積時,曲線下面積(AUC)就能達到74%。而在使用隨機法篩選出的HPF分析中,T細胞腫瘤侵潤和ICI應答沒有顯著相關性。
PD-L1-表型的巨噬細胞 (CD163+PD-L1-) 和癌細胞則與ICI應答成負相關 ,在熱點或隨機法選取~30-50%的總切片面積時,AUC達到73-76%。

不同細胞亞型對ICI應答的預測程度
用「熱點法」篩選出整個切片30%的HPF之後,研究者通過單變量分析發現了十個與ICI應答相關的特徵(P < 0.05);邏輯回歸分析在原有樣本里達到了92% AUC的預測率,在驗證樣本中也高達88%。

mIF檢測出多個因素與ICI應答相關;通過邏輯回歸分析,多因素mIF檢測在兩組獨立的黑色素瘤樣本中都達到了很高的應答預測
最後,研究者們將患者分為三組進行了生存分析:
– 免疫反應較差:在三個負相關特徵里的至少一種有着最高細胞密度
– 免疫反應較好:在七個正相關特徵里的至少一種有着最高細胞密度
– 免疫反應中等:以上兩種都不是/十個相關特徵的細胞密度水平都處於中等
三組免疫表型在驗證樣本的Kaplan Meier分析中對總生存期和無進展生存期都做到了準確的預測(OS P = 0.036;PFS P = 0.024)。

(C)三組患者在mIF腫瘤成像中的表達區別(D)Kaplan-Meier生存分析
Taube團隊的這篇論文首次通過將mIF的流程標準化推進了mIF在發現生物標誌物和臨床預測中的應用。
僅用六種熒光標記,AstroPath平台就實現了黑色素瘤ICI標誌物發現和患者生存預測。他們還表示,未來可以嘗試減少標記數量而增強mIF在臨床上的實用性,或嘗試其他免疫調節標記物來進一步分析對免疫療法產生耐藥性的腫瘤微環境。
未來,這種半自動化數據處理,減少人為干預的研究思路,或許可以進一步在多光譜組織成像學和細胞學中得到發揮。
參考文獻:
[1].Berry S, Giraldo NA, Green BF, et al. Analysis of multispectral imaging with the AstroPath platform informs efficacy of PD-1 blockade. Science. 2021;372(6547):eaba2609. doi:10.1126/science.aba2609
[2]. Sunshine J, Taube JM. PD-1/PD-L1 inhibitors. Curr Opin Pharmacol. 2015;23:32-38. doi:10.1016/j.coph.2015.05.011
[3]. Taube JM, Galon J, Sholl LM, et al. Implications of the tumor immune microenvironment for staging and therapeutics. Mod Pathol. 2018;31(2):214-234. doi:10.1038/modpathol.2017.156
[4]. Lu S, Stein JE, Rimm DL, et al. Comparison of Biomarker Modalities for Predicting Response to PD-1/PD-L1 Checkpoint Blockade: A Systematic Review and Meta-analysis. JAMA Oncol. 2019;5(8):1195-1204. doi:10.1001/jamaoncol.2019.1549